Стимулятор спинного мозга и нейропатические боли
Оборудование нейростимуляции для лечения нейродегенеративных заболеваний
Консервативное лечение при разрушении нейронов головного мозга не имеет выраженного положительного эффекта. Поэтому разработка немедикаментозных приборов набирает обороты. Конечно, это не терапия болезни, но метод позволяет сохранить активность оставшихся клеток.
Приборы при транслингвальной нейростимуляции головного
мозга
Для транслингвальной стимуляции используется прибор PoNS. Он разработан в США, имеет регистрационное удостоверение. Применяется методика для лечения Паркинсона, рассеянного склероза. Метод дает эффект при ДЦП, последствиях инсульта и параличах любой локализации.
Brainport
использует
технологию нейросенсорного замещения. Для передачи информации в мозг
применяется зона на кончике языка. Там сосредоточено максимальное количество
чувствительных окончаний. В область головного мозга по нейронам из языка
передается кодированный сигнал. Благодаря ему невидящие люди могут «видеть».
Brainport
balance – это
второй продукт, использующий транслингвальную передачу сигнала. Благодаря ему у
пациентов с нарушением вестибулярных функций сохраняется равновесие. Для работы
применяется сам прибор и акселерометр. По отклонению головы пациент может
судить об изменении положения тела.
Нейропорт был разработан российскими учеными. В основе методика аппарата Brainport, однако, проведены некоторые улучшения. Например, отсутствует необходимость перепрограммирования пластины.
Нейростимулятор
На рынке за последние несколько лет появилось более 20 приборов для стимуляции. Это и чрескожная, и имплантируемая форма аппаратов. Проведем их краткий обзор.
SpectraWaveWriter
Метод позволяет установить под кожу аппарат, который
посылает импульсы в головной и спинной мозг. Прибор настраиваемый. Его можно
включить, выключить и изменить испульсацию.
Nevro
Аппарат ставится в спинной мозг, а управление вживляется
под кожу. Однако, процедура настолько проста, что ее можно проводить в
амбулаторных условиях. А также фирма предлагает тестовый период прибора. Во
время него стимулятор можно носить на коже, пробуя его действия.
StimWave
Его небольшие размеры позволяют имплантировать стимулятор в
любом отделе. Заявленные пропорции аппарата меньше спички или булавки.
Cefaly
Это устройство в виде обруча. Оно не только стильно
смотрится. Прибор дает возможность лечить мигрень. При этом пациенты могут
полностью забыть о таблетках и капсулах.
Электроды для стимуляции
В приборе для нейростимуляции имеются как минимум два электрода. Это анод и катод. Первый возбуждает нейроны головного мозга. Он уменьшает разницу потенциалов на мембране и улучшает проведение импульса. Катод оказывает тормозящее действие на клетки мозга.
Важный фактор для лечения и профилактики заболеваний — это место установки катода и анода. При глубокой стимуляции мозга или лечении хронической боли электроды имплантируются в тело. Их надежная фиксация очевидна. Однако, бывают и смещения проводников. В этом случае эффект от лечения может быть утрачен. Потребуется новая операция.
Нейропорт
Этот прибор необходим для стимуляции ствола мозга через рецепторы. Они располагаются на кончике языка. От них возбуждение проходит по лицевому и тройничному нерву. А потом сигнал попадает в ядра эти черепных нервов и расходится по всему мозгу. Наибольшую стимуляцию получают структуры, расположенные в стволе мозга.
Нейропорт является отечественным прибором. Его цена около 60000 рублей. Для сравнения аппарат из США доступен за 7000 долларов. Сферы использования разнообразны:
- Восстановление после инсульта;
- Черепно-мозговая травма;
- Болезнь Паркинсона;
- Рассеянный склероз;
- ДЦП.
Обзор лидеров рынка
| PoNS | Производство Канада | Эффективен для транслингвальной стимуляции при болезни Паркинсона, Альцгеймера и рассеянном склерозе. Используется для восстановления после инсультов. |
| Brainport | Производство США | Имеются программы для восстановления равновесия. Эффективны тренировки при шаткости и нарушения ходьбы в поздних стадиях болезни Паркинсона. А также при рассеянном склерозе и паркинсонизме. Применяется для людей, утративших зрение. |
| Neiroport | Производство Россия | Аналог оригинальных приборов. Имеет аналогичные показания. |
Основные причины и исследования болевого синдрома
Болевой синдром у них носил нейропатический характер и обладал клиническими признаками, характерными для этого вида боли (гиперестезия, гиперальгезия, гиперпатия, аллодиния). Во всех случаях боли носили стойкий фармакорезистентный характер на нестероидные препараты, антиконвульсанты и антидепрессанты; ни один пациент из нашей группы не принимал наркотические аналгетики.
Интенсивность болевых ощущений оценивалась по визуально аналоговой шкале (VAS), у всех пациентов показатели VAS были выше 5 баллов. Также мы оценивали состояние восприятия боли пациентом по уровню удовлетворения (level of satisfaction) в дополнение к VAS, то есть больных спрашивают, насколько, по их мнению, улучшилось их состояние (насколько уменьшилась боль) — и иногда степень улучшения не коррелирует с цифрами VAS.
Например, больной говорит, что его боль снизилась с 6 баллов до 4 — получается 30% улучшение. Но при оценке уровня удовлетворения (level of satisfaction) он заявляет, что боль на 70% меньше — это, скорее всего, связано с нелинейным характером VAS, то есть 2/10 это не 20% от 10/10, а где-то процентов 5 в восприятии больного.
Все пациенты подверглись двухэтапному хирургическому вмешательству. На первом этапе пациентам имплантировался один электрод (в 4 случаях два эпидуральных электрода) в заднее эпидуральное пространство под местной анестезией (Pisces Quad Plus; PiscesZQuadPlus; Resume II, Medtronic). Электроды вводили пункционно (54 наблюдений) или устанавливали открытым способом (8 случаев).
Сразу на операционном столе выполнялась тестовая стимуляция, оценивался характер возникающих парестезии, зона распространения последних, что позволяло скорректировать положение электрода. Средняя продолжительность тестового периода составила 5 дней.
На втором этапе пациентам в условиях общей анестезии выполнялась имплантация подкожного программируемого генератора импульсов (Itrel 3; Synergy, Medtronic). Электрод соединялся с генератором с помощью тонкого кабеля-удлинителя. Затем выполнялось программирование генератора.

В тестовом периоде у 52 пациентов (83,9%) получен хороший противоболевой эффект, подобраны параметры стимуляции (полярность электродов, частота, длительность и амплитуда импульсов). У 10 пациентов (16,1%) в тестовом периоде не удалось добиться уменьшения интенсивности болевого синдрома. У пациентов с тест-негативным периодом в условиях местной анестезии удаляли эпидуральный электрод и генератор не имплантировали.
Механизм работы
 Пораженный участок плохо проводит нервные импульсы — аппарат доносит их до центров головного мозга
Пораженный участок плохо проводит нервные импульсы — аппарат доносит их до центров головного мозга
С болевыми ощущениями сталкивался каждый человек хоть раз в жизни. Нередко они локализуются в зоне спины. Если не лечить провоцирующее заболевание, симптом приобретает хроническое течение, сказываясь на психологическом, эмоциональном и физическом состоянии.
Не все спешат обращаться к врачу при наличии постоянных болей, боясь, что полноценное лечение не поможет избавиться от дискомфорта. Для снижения интенсивности боли в современной медицине имеется множество способов, например, медикаментозные с использованием сильных анальгетиков. Некоторые психические и нервные заболевания лечат методом вербальной терапии – электростимуляцией.
Как работает имплантация временных электродов для нейростимуляции спинного мозга, до сегодняшнего дня выяснено не до конца. Установлено, что при невропатических болях стимулирование спинного мозга способствует локальным нейрохимическим изменениям в отростках, что вызывает подавление гиперэксцибильности нейронов.
Соответствующими исследованиями доказана возможность высвобождения серотонина при стимуляции и подавление активности раздражающих аминокислот – аспартата и глютамина. При ишемической боли в ногах и руках анальгетический эффект обусловлен восстановлением нормального процесса обеспечения клеток кислородом. В результате снижается тонус сосудов, расширяется их просвет, устраняется спазм.
Нейропатический стимулятор оснащен следующей системой:
- импульсным генератором;
- пультом управления;
- электродами;
- соединительными проводами.
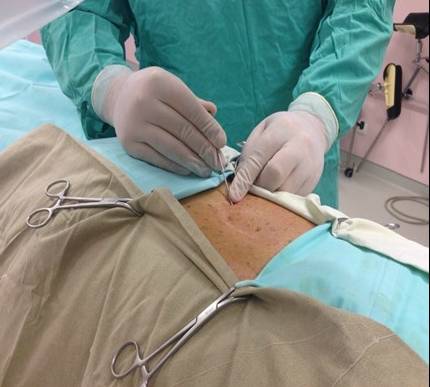 Устройство вводят под местным наркозом через небольшой разрез
Устройство вводят под местным наркозом через небольшой разрез
Генератор имплантируют чрескожно. Механизм действия имеет сходства с приемником радиочастот, который управляется из внешнего модуля. Это имплантируемый импульсный генератор, зарядка которого происходит с помощью батареи бесконтактно. Не требуется хирургическое вмешательство для замены батарейки.
Пульт предназначен для управления приемником радиочастот (включения и выключения). В нем присутствует легко заменяемая батарея.
Электроды – металлические пластины с общим выводом (катетером или сужающейся пластиной в форме весла). Микрополяризация может осуществляться с помощью биполярных и мультиполярных электродов.
Перкутанные электроды (с выходом в виде катетера) имплантируют под местной анестезией, используя седативные препараты в минимальном объеме. Это способствует оптимизации процесса внедрения стимулятора и снижению риска нейротравмы.
Больная спина синдром многих заболеваний
Несмотря на то что боли в области поясницы зачастую являются симптомом протекания иного заболевания, все чаще можно услышать, как ученые говорят, что хроническая боль является проблемой и сама по себе.
Хронической болью называют боль, которая продолжается не менее трех месяцев. Она возникает, когда болевые сигналы, идущие к мозгу по нервным волокнам, сохраняются, даже если источник боли исчез.
Дети Наргиз Закировой не поедут в Россию
Сара устала терпеть насмешки людей из-за веса. Через год они ее не узнали
3 типа людей в отношениях, которые больше других защищают свою половинку
Оценки за 2016 год от центров по контролю и профилактике заболеваний (CDC) предполагают, что около 1 из 5 взрослых в Соединенных Штатах живет с ней, при этом около 8 % имеют хроническую боль высокого уровня.
Общая годовая стоимость лечения этого синдрома в США, включая стоимость медицинского лечения и программ инвалидности по потере производительности, оценивается примерно в 560 миллиардов долларов.

Разновидности электростимуляции
Восстановление организма пациента в период реабилитации методом электростимуляции проводят несколькими способами:
- функциональной электростимуляцией;
- эпидуральной стимуляцией;
- интраспинальной микростимуляцией.
Механизм действия функциональной электростимуляции связан с использованием курсов влияния электрическими токами, что позволяет вызвать мышечные сокращения и движения, необходимые для выполнения конкретных задач. Активизация мышц происходит вследствие стимуляции двигательных точек.
Функциональная электростимуляция – наиболее распространенный метод лечения последствий позвоночно-спинномозговой травмы. Чаще используют накожный способ расположения электродов, в связи с чем стимуляцию называю неинвазивной.
 Более сложное оборудование способно научить парализованного ниже поясницы человека ходить и стоять
Более сложное оборудование способно научить парализованного ниже поясницы человека ходить и стоять
Если наблюдается нижняя параплегия (паралич обеих ног), требуется использование многоканальных устройств, предназначенных для восстановления шаговых движений и тренировки стояния. Накожные электроды стимулируют малоберцовый нерв, четырехглавую мышцу бедра, ягодичные мышцы.
Микрокомпьютер обеспечивает отхождение стимулирующих импульсов в данные отделы, что создает условия для выполнения разгибания ног, удержания в одном положении, сгибания и разгибания голеностопных суставов при инициации ходьбы.
Методика эпидуральной электростимуляции спинного мозга заключается в воздействии на корешки специальными электродами. Генератор имплантируют чрескожно в нижний брюшной отдел или ягодицы. Управление происходит с помощью пульта.
Если сравнивать эпидуральный метод с функциональным, последний предполагает временное применение, то есть курсами, а первый – долговременное использование. Действие эпидуральной стимуляции направлено на снижение спастичности, появление двигательных реакций в конечностях.
Интраспинальная микростимуляция обеспечивается за счет встраивания микроэлектродов в спинной мозг. Клинические случаи инвазивной стимуляции у людей на сегодняшний день не зарегистрированы. Метод применяем пока только на животных.
Стимуляция спинного мозга: нейромодуляционный способ влияния на активность нервной системы
Стимуляция спинного мозга является одним из эффективных методов управления «трудной» болью и относится к нейромодуляционным способам влияния на активность нервной системы. Методы нейромодуляции — это малоинвазивные оперативные вмешательства, которые связаны с электрической и/или медиаторной стимуляцией различных отделов нервной системы.
Разработанные и внедренные в клиническую практику в 70-х годах прошлого века способы электроимпульсного воздействия на задние столбы спинного мозга открыли новые возможности противоболевой терапии. Используя хроническую электростимуляцию, можно получать желаемые клинические эффекты, не разрушая ткани, т.е. данная методика принципиально отличается от применяемых ранее деструктивных процедур, таких как нейротомия, ризотомия, миелотомия и т.д.

Технология хронической эпидуральной стимуляции задних столбов спинного мозга применяется в мире на протяжении 30 лет. В нашей стране до сих пор частота использования этого эффективного метода в лечении боли остается низкой.
Термин «трудной» боли не является строго академическим. Тем не менее, он часто используется в научных статьях, посвященных консервативным и хирургическим способам лечения хронической боли. Данный термин даже вынесен в название блестящей монографии отечественных авторов по функциональной нейрохирургии, недавно вышедшей в печать. Под термином «трудная боль» мы подразумеваем хронический медикаментозно-резистентный нейропатический болевой синдром.
Нейропатическая боль имеет четкое определение, принятое Международной Ассоциацией изучения боли. Это боль, вызванная повреждением того или иного отдела нервной системы. Данный вид боли имеет ряд признаков и симптомов, хорошо известных и описанных разными авторами: аллодиния (болевая реакция на не болевой стимул), механическая и/или термальная гипералгезия (избыточный ответ на болевой стимул), гиперпатия (усиление боли на повторное раздражение).
Также для нейропатической боли характерны вегетативные расстройства (снижение локальной перфузии тканей, гипер- и гипогидроз, локальный остеопороз). Кроме того, нейропатическая боль может усиливаться при психоэмоциональных нагрузках.
Прием обычных аналгетиков, как правило, не приносит облегчения пациентам, страдающим нейропатическими болевыми синдромами. Влияют на нейропатическую боль антиконвульсанты и антидепрессанты, но и они часто не приносят облегчения и обладают значительными побочными эффектами.
При хронизации болевого процесса нейропатическая боль сама становится «болезнью», зачастую вне зависимости от начального этиологического фактора. Таким образом, общим показанием для применения метода спинальной стимуляции являлось наличие у пациента длительно текущего болевого нейропатического синдрома, резистентного к различным видам консервативного лечения (медикаменты, медикаментозные блокады, физиолечение, акупунктура, психотерапия).
Начиная заниматься лечением данной группы пациентов, мы четко отдавали себе отчет в том, что вступаем в поле паллиативной медицины, так как радикально избавить длительно страдающих пациентов от интенсивных болей мы не сможем. Нашей целью являлось улучшить качество жизни больных с нейропатической болью, т.е. постараться помочь им эффективно «управлять» своей болью.
За период с февраля 2007 по апрель 2010 г. было прооперировано 62 пациентов с различными болевыми нейропатическими синдромами. Более половины общего числа больных (42 пациента) ранее перенесли операции по поводу поясничных дегенеративных компрессионных синдромов.
Другие нозологии представлены доброкачественными спинальными опухолями (5 пациентов), травмами нервов (5 пациентов), травматическими грыжами дисков на среднегрудном уровне (двое больных), два пациента с т.н. «уровневыми» болями при нижней параплегии в результате позвоночно-спиномозговой травмы на поясничном уровне, 3 пациента с т.н. постхирургическими синдромами (1- после торакотомии, 2 — после герниотомии с клиникой повреждения п. Illioingvinalis), 2 пациента с диабетической полинейропатией и 1 пациент с облитерирующим атеросклерозом нижних конечностей после серии шунтирующих и реваскуляризирующих сосудистых вмешательств.
Все пациенты, за исключением пациентов с диабетической полинейропатией, неоднократно оперированы ранее по поводу основного заболевания. Все пациенты длительно лечились у врачей различных специальностей (нейрохирургов, неврологов, физиотерапевтов). У всех больных применение консервативных методов лечения и дальнейшие хирургические операции оказались безуспешными.
Показания для применения SCS
Эпидуральная электростимуляция спинного мозга влияет на ряд болезненных синдромов. В особенности, делать ее рекомендуется при хронической доброкачественной боли нейропатической этиологии (возникает в результате повреждения периферических нервов или корней). Полезна процедура при смешанной боли, содержащей нейропатический и ноцицепторный компонент.

Проводить SCS рекомендуется при следующих состояниях:
- синдром постдизотомии, в клинике которого преобладает болезненность в нижних конечностях;
- спастика;
- фантомная боль;
- ДЦП;
- комплексный региональный болевой синдром (ранее называвшийся альдодистрофическим синдромом) II типа; меньше подходит I тип;
- болезненный синдром после повреждения периферических нервов, сплетений;
- постгерпетическая невралгия;
- полинейропатия;
- стенокардия без возможности медикаментозного или оперативного лечения;
- ишемическая болезнь нижних конечностей III-IV степени по Фонтейну.
Основные исследования болевого синдрома по шкале VAS
Все пациенты с положительным тест-периодом отмечали появление чувства легкого покалывания и/или теплых волн в той части тела, где они обычно чувствовали боль. Эти ощущения были комфортными для пациентов. Сразу после операции у этой группы больных показатели VAS были не выше 5 баллов, также показатели уровня удовлетворения были в пределах 50-90%. Катамнез в нашей группе больных составил от 1 до 26 месяцев.
Шестеро пациентов (9,7% от общего числа больных и 11,5% от пациентов с положительным тестовым периодом) в сроки 15-21 месяцев после операции стали отмечать уменьшение противоболевого эффекта от проводимой стимуляции. Мы расценили это явление как «эффект привыкания к стимуляции». Таким образом, в нашей серии из 62 пациентов стойкого эффекта от противоболевой стимуляции удалось добиться у 46 больных (74,2%). Возможно, с увеличением срока наблюдения за оперированными больными мы получим уменьшение количества хороших результатов.
Таким образом, отбор пациентов для применения данной методики должен производиться с крайней тщательностью в строгом соответствии со следующими критериями:
- инвалидизирующий характер болевого синдрома;
- отсутствие грубых психологических расстройств у пациента;
- пациент должен адекватно оценивать свое состояние и возможности предстоящего хирургического лечения;
- наличие хорошего противоболевого эффекта в тестовом периоде;
- пациент в ходе операции и в послеоперационном периоде должен быть способен правильно выполнять инструкции врача и периодически проходить контрольное обследование
.
Этот метод не является панацеей от всех бед, а его клиническая эффективность, по данным масштабных и многолетних исследований, не превышает 55-70%, т.е. потенциальный процент фиаско довольно высок. Ввиду этого тщательный отбор пациентов является пусть не абсолютной, но все же страховкой от получения отрицательного результата и разочарования как пациента, так и хирурга.
Ссылки по теме:
- Cтеноз спинномозгового канала
- Эффективность эпидуральной электростимуляции при миелопатии различного генеза
- Опыт применения хронической эпидуральной нейростимуляции
Также стоит почитать:
Имплантация SCS
Фактическая имплантация системы нейростимуляции состоит из 2-х этапов.
На первом этапе с помощью иглы Туохи через небольшой разрез электрод под рентгенологическим контролем помещается в эпидуральное пространство спинного канала. Вхождение в эпидуральное пространство и место стимуляции должны находиться на расстоянии примерно 2-3 позвонков друг от друга. Эта фаза проводится под местной анестезией и аналгоседацией, т.к. требует сотрудничества пациента. Конечное расположение электрода зависит от локализации боли и парестезии, указанной больным:
- для контроля болезненности в верхних конечностях проксимальный конец электрода располагается в области C3-C7;
- для контроля боли нижних конечностей – в области Th11-Th12;
- при постдискотомическом синдроме, боли в спине – Th8-Th10;
- при стенокардической боли – в области C8.
При односторонней боли электрод помещается на болезненную сторону, при двусторонней боли – располагается в средней линии или имплантируется 2 электрода. После размещения электрода в эпидуральном пространстве его дистальный конец соединяется с внешним источником стимуляции. После начала стимуляции пациент испытывает параэстезию в определенной области, а электрод сдвигается до тех пор, пока парестезии покрывают всю область сознательной боли.
За этим следует несколько дней пробного периода, когда пациент и врач посредством внешнего генератора удостоверяются в эффективности действия нейростимулятора. Если стимуляция успешна, т.е. обеспечивает уменьшение болезненности, как минимум, на 50%, следует 2-я фаза имплантации.

В ходе 2-го этапа при общей анестезии электрод интернализуется, а генератор импульсов (IPG) внедряется в небольшой подкожный карман. Параметры стимуляции телеметрически с помощью медицинского программатора передаются через кожу; они могут в любое время изменяться, адаптироваться к потребностям пациента. Больной получает маленький ручной программатор, которым включает и выключает устройство, изменяет интенсивность и частоту электрических импульсов в пределах диапазона, установленного врачом.
Электрод фиксируется в спинномозговом канале путем образования спаек в течение 4-6 недель. На протяжении этого периода человек ограничен в определенных ежедневных действиях (ношение груза весом более 2 кг, поднятие рук над головой, наклоны, вращение туловища). Пациент не реже 1 раза в 6 месяцев осматривается врачом; также проводится проверка правильности работы устройства.
Показания и противопоказания
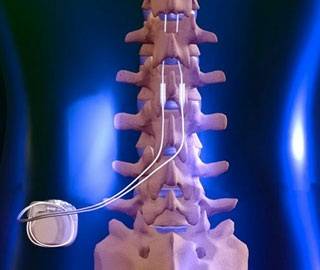 Стимуляцию нервов проводят для снятия болей при лечении патологий позвоночника
Стимуляцию нервов проводят для снятия болей при лечении патологий позвоночника
Трансвертебральная микрополяризация спинного мозга улучшает общее состояние и устраняет боль в период лечения следующих заболеваний спинного мозга и нервов:
- синдрома неудачно прооперированного позвоночника: операция на спинной мозг может вызвать состояние, характеризующееся персистирующими или рецидивирующими радикулярными синдромами – болью, онемением, слабостью мышц и др.;
- радикулита спинного отдела с болевым синдромом или без него;
- диабетической невропатии;
- постгерпетической невралгии;
- поражения периферического нерва с развитием невропатического болевого синдрома;
- рефрактерной стенокардии;
- болезни Рейно, облитерирующего эндартериита – сосудистых заболеваний нижних и верхних конечностей;
- стеноза позвоночного канала.
Трансвертебральный нейростимулятор встраивают после травмы спинного мозга или позвоночника (сильного ушиба и др.). Также метод эффективен в лечении спастической боли при нарушении работы органов таза, последствий инфаркта нейрогенного характера. Нейротехнологию используют после операции по удалению опухоли на спине (в спинном мозге, ином отделе).
Несмотря на эффективность способа, делать нейромодуляцию запрещено при наличии следующих противопоказаний:
- развитие тяжелого соматического заболевания;
- инкурабельная лекарственная зависимость;
- развитие психического заболевания, наличие суицидальных попыток в анамнезе;
- снижение интеллектуальных способностей у больного, задержка психического развития (ЗПР), например, при ДЦП, что выступает препятствием к применению системы электростимулирования;
- наличие активной инфекции в области, где планируется операция и работа электростимулятора.
Применениенейростимуляции при НДЗ
Причина разрушения нейронов у возрастных пациентов так и не раскрыта. Однако, появились методы, которые помогут с ней справиться. Применение электростимуляции эффективно для болезни Паркинсона, Альцгеймера и других видов деменций. Эффективна методика при инсультах, церебральной ишемии и расстройствах настроения. Но есть и ограничения применения метода.
Нейростимуляция
при болезни Паркинсона
Для лечения тяжелых форм заболевания и лекарственной
устойчивости применяется глубокая стимуляция структур мозга. При этом электроды
вживляют в нервную ткань в область базальных ганглиев. С помощью импульса
стимулируются зон мозга, отвечающие за плавность движения. Существенное улучшение
наступает сразу после операции
Возможные причины неэффективности лечения – это смещение
электродов или неверная локализация их установки. В таком случае проводят
реимплантацию приборов.
Нейростимуляция при других нейродегенеративных заболеваниях
Методику с успехом применяют при рассеянном склерозе, диабетической полинейропатии, деменциях. При РС эффективна транслингвальная стимуляция. Это новый способ работы со стволовыми структурами. При этом электроды накладываются на кончик языка. А импульсация доходит до стволовых структур и возбуждает расположенные рядом зоны. При рассеянном склерозе удается восстановить походку и речи даже в случае тяжелого поражения.
Плюсы и минусы
Плюсы методики в том, что многие утраченные функции можно
восстановить с помощью немедикаментозных методов. При этом не страдают внутренние
органы пациента. Не нужно ежедневно принимать таблетки
Важно, что
электростимуляция позволяет снизить дозу лекарственных средств. А возможна и
полная независимость от медикаментов
Минусы метода в том, долгосрочные исследования отсутствуют.
Возможен частичный эффект, смещение электродов с потерей терапевтической
функции. Глубокая стимуляция мозга – это операция, которая связана с рисками.
Это инфицирование, наркоз, реакция отторжения имплантат.
Меры предосторожности
Лечение должно проводиться под контролем специалиста.
Например, смещение электродов при чрезкожной стимуляции может привести к
нарушению результатов. Не следует применять лечение без соответствующего
назначения врач.

Отдаленное воздействие постоянного и переменного тока на
мозг не изучено. Нервная ткань – это сложная структура. В ее состав входят не
только нейроны. Ученые пока не могут предположить, как отреагируют другие
клетки мозга на хроническое воздействие током.
Примеры и результаты
Стимуляция позволяет эффективно справляться с болью,
тремором, симптомами дискинезии. Результаты лечения в исследовании таковы:
- Около 60% пациентов полностью избавляются от симптомов;
- В 13-18% признаки возвращаются снова, но в легкой форме;
- На лечение не реагирует около 3-5%, это в основном связано нарушение технологии имплантации;
- В 90% случаях удается уменьшить дозу лекарственных препаратов.
Подготовки к операции по имплантации электродов
Поскольку в результате операции в организм больного попадёт и будет длительно размещено инородное тело, необходимо проведение профилактических мероприятий для исключения риска инфицирования и развития иных осложнений:
- обследование общего состояния больного на предмет переносимости оперативного лечения (сердечно-сосудистой и дыхательной системы, иммунного статуса и фоновых заболеваний);
- выявление возможных латентных инфекций методом бакпосева соскоба из носа, глотки, промежности (особую опасность представляет Staphylococcus aureus);
- антибиотикотерапия (при выявлении инфекций одновременно оценивается чувствительность бактерий к разным группам антибиотиков, что учитывается при выборе препаратов);
- согласование с пациентом возможной локализации подкожного генератора.
Послеоперационный период
- Больной проведет в послеоперационном отделении 1-2 часа.
- Хирург объяснит семье течение операции и последующие этапы лечения.
- Обычно в тот же день пациент может быть выписан из больницы и ему разрешеноперенести полет или переезд на машине.
Если в результате проведённой операции боли значительно уменьшатся, то вместо наружного источника энергии будет установлен постоянный внутренний генератор, и пациент самостоятельно сможет регулировать. его переключение.
Сверхтонкое лезвие
Ультразвуковой костный скальпель Misonix
- выполнение разреза практически без усилий
- высокая точность прямых и изогнутых разрезов
- минимальное повреждение костной ткани
- снижается уровень травматизации
Подробнее
Диагностика высшего уровня
Интраоперационный компьютерный томограф О-АРМ
- мобильная конструкция томографа
- отсутствие погрешности
- безопасность оперативного лечения
- исключает необходимость использования дополнительных средств рентген-контроля
Подробнее
Максимальное внимание
Навигационная станция
- процесс операции в режиме реального времени
- вывод на экран результатов исследования пациента
- хирург отслеживает траекторию движения инструмента
- определяет соттветвие хода операции
Подробнее
 МИР ЛОГИКИ
МИР ЛОГИКИ